发布日期:2019-03-03
医学版块简单说即药物应用从动物到人的过程。临床前研究包括药效学、药代动力学以及毒理学安全性评价研究等。临床阶段需要在人体上进行试验,因此药物进入临床研究前必须得到国家药品监督管理部门的审批。在中国,新药的研发机构需要向国家药品监督管理局(National Medical Products Administration,NMPA)提交新药临床申请(investigational new drug, IND),获得许可后才能进行人体临床试验。临床研究还需要分为四个阶段:Ⅰ期临床试验,Ⅱ期临床试验,Ⅲ期临床试验和IV期临床研究(药物上市后监测)。
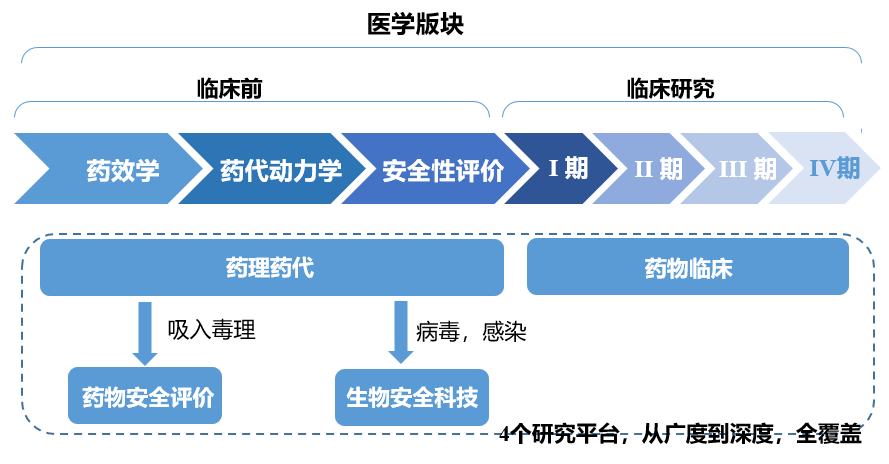
药物临床研究平台主要进行各类新药I期、II期、III期、IV期临床试验、上市后再评价、中药保护品种临床试验、一致性评价、临床研究项目的第三方稽查、医疗器械临床研究、保健食品临床研究、特殊医学用途配方食品临床研究、技术咨询与服务(含产品顶层设计、医学学术推广、专家咨询会议、申报资料撰写等技术支持)。实施临床项目涉及领域广泛,包括:肝病、精神、神经、风湿、心脑血管、内分泌、消化、肿瘤、皮肤、抗感染、泌尿、呼吸、妇科、儿科、乳腺、血液、眼科等。

扫一扫关注微信